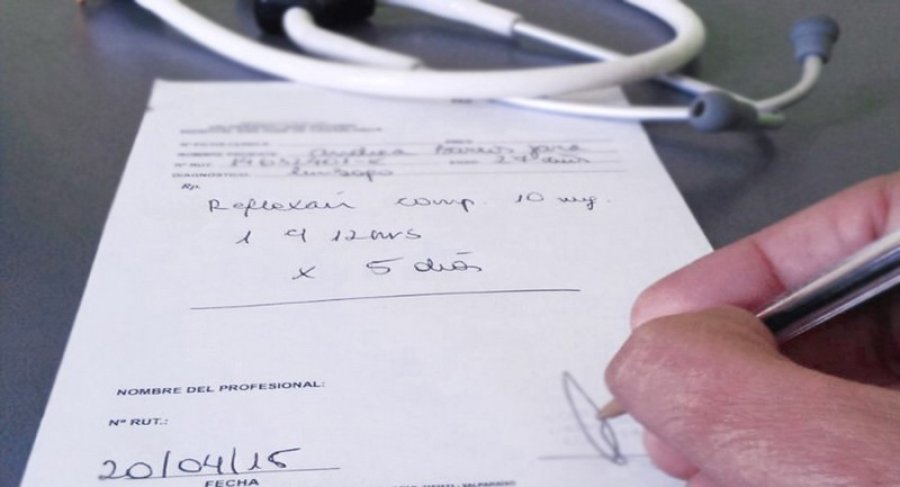
A días de que comenzara el nuevo año, la publicación del Decreto de Necesidad y Urgencia (DNU) 70/2023, el pasado 20 de diciembre, estableció una serie de modificaciones a normas vigentes, entre las que se encuentra el artículo 2 de la Ley N° 25.649, de Utilización de medicamentos por su nombre genérico. Este cambio establece que “toda receta o prescripción médica deberá efectuarse en forma obligatoria expresando exclusivamente el nombre genérico del medicamento o denominación común internacional que se indique, seguida de forma farmacéutica y dosis/unidad, con detalle del grado de concentración”.
Ante este situación, la Academia Nacional de Medicina (ANM) y 48 entidades médicas cuestionaron con dureza estos cambios en la prescripción de fármacos. Es que, según el comunicado emitido en las últimas horas, la prohibición de incluir en las recetas la sugerencia de marcas comerciales de medicamentos por parte de los médicos, junto a la denominación genérica, “perjudica a los pacientes” y “limita la responsabilidad del médico”.
Con el transcurrir de las horas, nuevos cuestionamientos se sumaron a los cambios planteados por el DNU, así lo señalaron a Infobae desde la Cámara Industrial de Laboratorios Farmacéuticos (CILFA) y referentes de los médicos de la Sociedad Argentina de Lípidos y la Federación Argentina de Sociedades de Endocrinología.
De acuerdo a lo expresado por la ANM, el eje de la discusión se centra en que “en la Argentina no existen pruebas de bioequivalencia y biodisponibilidad en la gran mayoría de los productos farmacéuticos”, los cuales solo están destinados a un grupo de fármacos específicos para el tratamiento de algunas patologías. Es decir que, en la mayoría de estos productos farmacéuticos, no puede garantizarse el mismo nivel de eficacia y seguridad entre ambas drogas (la denominada como madre y el genérico). Esto es especialmente sensible en los casos de pacientes oncológicos, por citar un ejemplo advertido por los expertos.
Algunas de las entidades firmantes son: la Asociación Argentina de Oncología Clínica, la Sociedad Argentina de Cardiología, la Federación Cardiológica Argentina, el Colegio Argentino de Cardiología, la Sociedad Argentina de Infectología, la Sociedad Argentina de Hematología, la Sociedad Argentina de Urología, la Sociedad Argentina de Mastología, la Sociedad Argentina de Dermatología, el Colegio Argentino de Cardioangiólogos Intervencionistas, la Sociedad Argentina de Cirugía Plástica y Reparadora, la Sociedad Argentina de Ginecología Infanto Juvenil, la Sociedad Argentina de Patologías de Urgencia y Emergentología, la Sociedad Argentina de Neurocirugía Pediátrica, y entre otras.
En ese sentido, Mazzei aclaró un punto que suele provocar confusión: “Cuando se habla de medicamentos genéricos en la Ley N° 25.649 vigente desde 2002, se habla de la prescripción por nombre genérico que es la denominación común internacional, es decir la droga (o principio activo). Pero, en rigor, los medicamentos genéricos son aquellos avalados por pruebas que demuestran que tienen la misma potencia y efectividad que el producto original y eso en Argentina no ocurre en la mayoría de los casos”. Al tiempo que aclaró que, desde ese año, “hubo laboratorios (fabricantes de genéricos) que hicieron pruebas, pero no todos”.
Es por este motivo que el presidente de ANM consideró que los médicos deben conservar la potestad de sugerir medicamentos en la receta y que, en segundo lugar, en el futuro se debe debatir y establecer una Ley de genéricos “en la que todos los productos deban presentar pruebas de biodisponibilidad y bioequivalencia, ya que la ANMAT hoy sólo se lo exige a 68 productos genéricos de los disponibles, en un mercado con miles de productos farmacéuticos”.
Ante la consulta de Infobae, el doctor Pablo Corral (MP 93.559), presidente de la Sociedad Argentina de Lípidos, se manifestó “en contra de esta determinación”. “Para que nosotros, los médicos, podamos prescribir medicamentos genéricos deberíamos tener el sustento científico, tanto en lo que es bioequivalencia y biodisponibilidad. Estos son estudios que se hacen para comparar la droga patrón con los genéricos y eso en Argentina no existe”, sostuvo el médico internista y lipidólogo.
“No existen genéricos que tengan estudios comprobados de que sean similares en eficacia y seguridad a la droga madre o patrón, en este caso -prosiguió-. Entonces, uno que es el responsable por la prescripción de un medicamento, en cuanto a la salud del paciente y a los aspectos potencialmente judiciales, debería tener la potestad de decir: ‘Este es el genérico y recomiendo esta marca comercial o este grupo de marcas comerciales’. Y eso es lo que intenta derogar el DNU. Existe la Ley de Medicamentos Genéricos del año 2002, que avala y creo que ha funcionado bien en estos más de 20 años. Pero me parece que para modificar esto deberíamos tener una estructura, reitero, avalada científicamente. Y no la tenemos. No estoy en contra de que en algún momento se genere, pero no es el momento y no están dadas las condiciones para que eso ocurra”.
Ante la autoridad que se le da al farmacéutico para que decida qué producto se dispense al paciente, Corral sostuvo que esto “también atenta contra la potestad del médico, porque es el médico el que pone el sello y la firma. Y, también, quien se hace responsable por el medicamento que el paciente reciba”.
Y cerró: “Este punto del DNU, estimo, está redactado por personas que no entienden de bioequivalencia en función de los fármacos. La cuestión hubiese sido adecuada, en tanto en cuanto, se hubiesen consultado a las diferentes sociedades científicas y se hubiese involucrado a los distintos representantes de éstas para poder, en este caso, generar algún tipo de recomendación extra. Por algo, casi todas las sociedades científicas han manifestado preocupación de que se aplique el artículo del DNU ante la falta básica de estructura científica que avale la utilización, hoy en Argentina, de medicamentos genéricos, y de que se tengan la acabada evidencia de seguridad y eficacia, en comparación de la droga madre o patrón”.
Juan Patricio Nogueira (MN 97.545), médico especialista en endocrinología y nutrición, investigador adjunto del CONICET y presidente de la Federación Argentina de Sociedades de Endocrinología (FASEN), indicó que es positivo que se aplique la ley genéricos “porque, según la Organización Mundial de la Salud, un medicamento genéricos es aquel que es completamente bioequivalente a la marca original. Es decir, es igual en su composición forma farmacéutica y biodisponibilidad”. Aunque aclaró: “En principio, estaría de acuerdo con el artículo, pero en la Argentina, la ANMAT no cumple con todas las normas de bioequivalencia para todas las drogas disponibles en el mercado”.
En palabras de Nogueira, “la modificación que propone el artículo 2 del DNU tendría un impacto directo al restringir la prescripción únicamente por el nombre del genérico el medicamento. Pero hay que hacer una aclaración: nuestro país no exige a todos los medicamentos la prueba de bioequivalencia y biodisponibilidad comparadas con la marca de referencia. Solo lo tiene principalmente para medicamentos relacionados a enfermedades neurológicas, demencias o infecciosas, para el resto las especialidades no tiene una obligación o no está del todo establecido”.
“Lógicamente - apuntó el experto-, cambia la práctica profesional en el aspecto en que deberíamos prescribir principios activos. Puede ser que esta medida, tras el decreto, exija a posteriori a la ANMAT a impulsar reglas de bioequivalencia y que eso se aplique exactamente en todos los medicamentos disponibles en Argentina. Eso es lo relevante de este decreto y este artículo 2 en relación a los genéricos, que deberán, a posteriori, reglamentarse a través de la ANMAT las bioequivalencias a todos los medicamentos”.
Gonzalo Camargo (MN 105.424, MP 451.230), especialista en Clínica Médica y Emergentología, Jefe de Emergencias en Sanatorio de la Trinidad Ramos Mejía y ex Presidente de la Sociedad Argentina de Emergencias, sostuvo por su parte a Infobae: “Se trabaja con ciertos medicamentos, de los cuales se conoce la droga y se está acostumbrado. Si se ve que el paciente anda bien, se sigue trabajando con ese tipo de medicación. Entonces, la idea de que el paciente solo, o con el farmacéutico, decida cambiar la medicación es un poco riesgosa, porque a veces sabemos que las composiciones no son iguales y cuando la crisis aprieta, la gente va a tratar de comprar el más económico, que no siempre es el mejor. Lo importante sería, obviamente, que los medicamentos sean accesibles a la mayoría de la población, con buenos resultados y buenos laboratorios”.
Desde la Cámara Industrial de Laboratorios Farmacéuticos (CILFA) indicaron que el DNU tiene varios problemas en lo que respecta a la prohibición de incluir las marcas de medicamentos en las recetas. “Desde el punto de vista sanitario, conforme a la regulación vigente en Argentina, en nuestro país no contamos con medicamentos genéricos en sentido estricto, es decir, intercambiables, sino únicamente con medicamentos similares, no sometidos a exigencias de bioequivalencia/biodisponibilidad, por lo que no necesariamente los medicamentos que contengan el mismo principio activo producen siempre el mismo efecto en los pacientes”, expresaron desde CILFA en un comunicado.
“Sólo un pequeño universo de principios activos tiene bioequivalencia aprobada por la ANMAT. Por tal motivo, la marca cumple una función esencial para los médicos. Al momento de recetar, el médico evalúa a los pacientes y trazan un diagnóstico en función de sus características e historia clínica. Simultáneamente, el médico toma en consideración las cualidades de los medicamentos existentes, la promoción médica y la información científica disponible”, agregaron.
En ese marco, según explicaron desde CILFA, las marcas de los medicamentos son las herramientas que permiten a los laboratorios trasladar la información y promoción médica al acto de prescripción “para llegar al paciente con intervención del médico y del farmacéutico. Las marcas de los medicamentos permiten entonces competir por calidad, ya que el médico sugiere en la receta una marca en virtud de la calidad del medicamento, como así también el paciente toma en cuenta dicha prescripción al momento de la dispensa en la farmacia, a fines de evaluar si prefiere sustituir o no el medicamento por otro similar (que no es lo mismo que genérico). Insistimos en que los medicamentos no son todos iguales, presentando no sólo diferencias a nivel productivo e institucional sino también respecto de sus riesgos, beneficios, interacciones y eventuales efectos adversos”.
“Desde el punto de vista internacional, la prohibición de consignar marcas en las recetas es contraria a los acuerdos de la Organización Mundial de Comercio, que impide la adopción de medidas que menoscaben la capacidad distintiva de las marcas. Es también contrario a las reglas de más de veinte tratados de protección y promoción de inversiones que obligan a otorgar un trato justo y equitativo a las inversiones, al tiempo que prohíben su expropiación indirecta por medio de medidas que las privan de su valor. Sería paradójico que la Argentina fuera demandada en el CIADI por este tema”, sumaron desde la cámara.
“Además, la reforma no tiene parangón en el mundo desarrollado y/o en vías de desarrollo a través de economías de mercado. Según nuestros registros, sólo en Cuba y Venezuela se prohíbe consignar marcas de medicamentos en las recetas. Existe una profunda contradicción entre los objetivos declarados del DNU vinculados con la economía de mercado, la desregulación y la libertad, por un lado; y la inclusión de una prohibición propia de economías dirigidas que reniegan de la competencia por precio y calidad, por el otro”, sumaron en el comunicado de CILFA.
Y finalmente se mostraron preocupados ante la posibilidad de que los medicamentos de venta libre se puedan comercializar fuera de las farmacias, según expresaron, “sin criterios profesionales o sanitarios, porque inevitablemente aumentarán los casos de medicamentos en mal estado por el mal manejo en su almacenamiento, cuidado y dispensa y el consecuente riesgo para la salud de los pacientes; y, por el otro, generará bocas de expendio no controladas por las que se comercializarán medicamentos falsificados o robados, lo que afortunadamente se encuentra muy controlado hasta el momento”.





















Compartinos tu opinión